医疗器械研发工程师入门知识,,机械设计基础知识,医疗器械开发流程大概分为八个步骤(产品需求、系统需求、研发设计、测试验证、型式检测、设计冻结、临床试验、注册拿证、机电部件开发流程)。这八个步骤完成后,一款新的医疗器械就可以获批上市了。首先是产品需求确定,这个是由产品经理来进行定义,主要通过市场的调研,临床应用场景,医生拜访,产品经理需要对产品的整个工作流行定义和澄清。产品经理的需求会传递给系统工程部,由系统工程师承接,然后降产品的需求转化为工程技术指标。这个过程中,系统工程师需要完成系统功能架构和组成部件的划分,除此之外,还需要输出法规和标准,风险安全性、可用性、可服务性。和可制造性等相关的需求来对系统进行约束,确保系统可以满足医疗器械的要求。
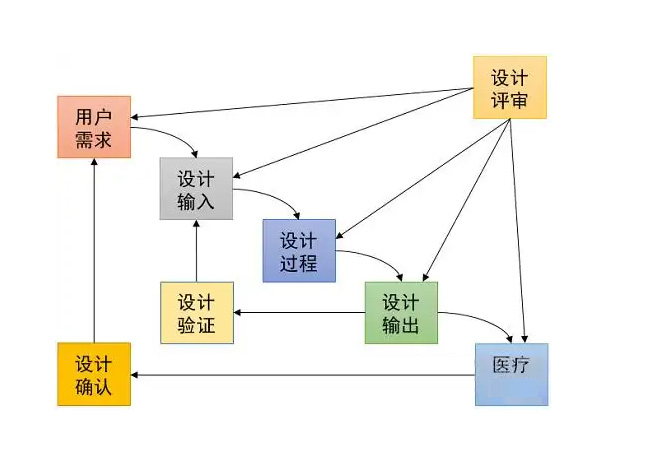
系统需求由器械研发工程师承接,器械研发工程师需要将系统需求转化为不见设计规范。并对系统指标进行分解。细化为不见设计的指标。并且定义这些指标的测试方法。然后进行部件结构的设计、打样验证和优化迭代工作。测试的目的是为了验证部件系统的设计是不是满足产品的要求。分为了不见测试、集成测试、系统测试、法规测试、风险测试、可用性测试、内部动物试验。都是为了不见跟系统的确认。确保设计要符合要求。这些测试项目都通过后就可以进行国家药监局的检测了。型式检测通过,需求文档、设计规范、物料验证、BOM、图纸、测试文档及报告、工艺SOP等冻结受控。将研发状态转换成为可以量产状态。小批量试产,为临床试验做好准备。生产的样机需要完成临床试验的验证。动物临床试验,临床数据分析等。动物试验是为临床试验做准备。通过临床试验、医生使用器械在病患身上做手术。确认系统功能满足临床使用要求。试验期间的临床数据和医生的反馈。作为下一代产品研发需求的输入。进行产品的迭代。临床试验通过后,提交临床数据和,型式检测报告,在国家药监局提交,注册申请,拿证获批后即可上市。医疗器械法规及标准,人机交互理论,常用工具跟软件。
联系人:13922709440 余先生
销售热线:0724-4016818
售后服务:19171569097
服务热线:400-800-8232
邮 箱:xianhao266@163.com
公 司:湖北省显浩装备科技有限公司
地 址:湖北省钟祥市南湖新区协企联盟产业园C6栋